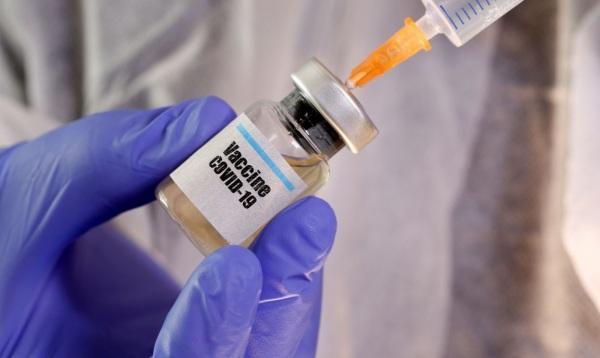
Após aprovação da Agência Nacional de Vigilância Sanitária (Anvisa) na última sexta-feira (3), o governo de São Paulo vai iniciar a fase 3 de teste em humanos da vacina contra o novo coronavírus, chamada de CoronaVac, no dia 20 de julho.
“A Anvisa autorizou o Instituto Butantan a iniciar os testes da CoronaVac, a vacina está sendo desenvolvida junto com o laboratório chinês. A partir da próxima segunda-feira (13), os voluntários já poderão se inscrever. A inscrição será obrigatoriamente para profissionais da saúde”, disse João Doria, governador de São Paulo. “Com a aprovação da Anvisa, começaremos o processo de testagem a partir do dia 20 de julho”, acrescentou.
Segundo Dimas Covas, diretor do Instituto Butantan, esta vacina contra o novo coronavírus é desenvolvida pela Sinovac, sediada na China, e é uma das mais promissoras do mundo, porque utiliza tecnologia já conhecida e amplamente aplicada em outras vacinas. É também uma das mais avançadas em testes. Ela já está na terceira etapa, chamada clínica, de testagem em humanos. O laboratório chinês já realizou testes do produto em cerca de mil voluntários na China, nas fases 1 e 2. Antes, o modelo experimental aplicado em macacos apresentou resultados expressivos em termos de resposta imune contra as proteínas do vírus.
“A fase 2 [de testes clínicos, feito na China] demonstrou a segurança e a eficácia da vacina. Após 14 dias da segunda vacinação, mais de 90% das pessoas vacinadas desenvolveram proteção. Então é uma vacina que tem um perfil de proteção elevado”, explicou.
Os voluntários para a CoronaVac serão selecionados entre profissionais de saúde, da rede pública ou privada, com mais de 18 anos, que não tenham tido covid-19 [a doença provocada pelo novo coronavírus] e que não estejam em teste para outras vacinas. Esses voluntários poderão se candidatar por meio de um aplicativo do Instituto Butantan, que deverá ser lançado na próxima segunda-feira (13). Os voluntários não poderão ter doenças instáveis [que afetem a resposta imune], distúrbios de coagulação e, as mulheres não poderão estar grávidas. “São esses profissionais que estão mais expostos e que vão permitir o desenvolvimento muito rápido do estudo clínico”, disse Dimas Covas.
Os testes com a CoronaVac serão realizados em 9 mil voluntários em centros de pesquisas de seis estados brasileiros: São Paulo, Brasília, Rio de Janeiro, Minas Gerais, Rio Grande do Sul e Paraná. A pesquisa clínica será coordenada pelo Instituto Butantan e o custo da testagem é de R$ 85 milhões, custeados pelo governo.
A vacina é inativada, ou seja, contém apenas fragmentos do vírus, inativo. Com a aplicação da dose, o sistema imunológico passaria a produzir anticorpos contra o agente causador da covid-19, a doença provocada pelo novo coronavírus. No teste, metade das pessoas receberão a vacina e metade receberá placebo, substância inócua. Os voluntários não saberão o que vão receber.
Segundo Dimas Covas, diretor do Instituto Butantan, caso os testes comprovem a eficácia da vacina, 60 milhões de doses iniciais estarão disponíveis para o Brasil pelo laboratório chinês até o final deste ano.
Esta é a segunda vacina que está sendo testada no Brasil. A primeira é a que está sendo produzida pela Universidade de Oxford, no Reino Unido.
Publicada em 06/07/2020
Fonte: Agência Brasil